Ticagrelor + Aspirine versus Aspirine seule en cas d’Infarctus Cérébral aigu ou d’Accident Ischémique Transitoire.
En cas d’Infarctus Cérébral (IC) ou d’Accident Ischémique Transitoire (AIT), le risque de récidive est approximativement de 5 à 10 % dans les premiers mois. L’Aspirine (ASA) est habituellement le traitement anti-thrombotique préventif utilisé, mais 2 essais thérapeutiques ont montré que l’association à l’ASA du clopidogrel réduisait le risque de récidive d’IC ou d’événement cardio-vasculaire dans cette population. L’activité du clopidogrel (CPG), antiplaquettaire bloqueur du récepteur plaquettaire P2Y12, nécessite une transformation hépatique en métabolite actif. Cette étape peut être défaillante dans 25 % des cas dans la population caucasienne et jusqu’à 60 % des cas dans la population asiatique.
Le ticagrelor (TCG) possède, lui, une action directe et réversible sur les récepteurs P2Y12 plaquettaires. Une étude (SOCRATES, Johnston SC, NEJM 2016) n’a pas montré de bénéfice du TCG comparé à l’ASA sur la récidive d’évènements cardio-neuro-vasculaires ou de décès. Cependant, un sous-groupe de patients ayant reçu de l’ASA dans les 7 jours précédents la randomisation a bénéficié d’une réduction des évènements vasculaires majeurs sous clopidogrel, laissant ainsi supposer que le bénéfice constaté pouvait être lié au CPG associé à la rémanence des effets de l’ASA pendant les premiers jours. Etant donné que le risque de récidive intéresse essentiellement le premier mois suivant l’événement initial, une période de traitement de 30 jours est considérée comme appropriée pour prévenir les récidives et/ou décès pour mener une étude associant le TCG à l’ASA en cas d’IC ou d’AIT non cardio-emboliques (Etude THALES).
METHODE
|
Design
|
Prospective, multicentrique, randomisée double aveugle 1:1, versus placebo, en intention de traiter. 414 sites dans 28 pays (Asie, Océan Pacifique, Amérique du Nord et du Sud, Europe).
|
|
Population |
Critères d’inclusion : Adultes ≥ 40 ans, IC mineur non cardio-emboliques (NIHSS ≤ 5), AIT à haut risque (ABCD2 ≥ 6) ou avec sténoses ≥ 50 % intra ou extra-crâniennes homolatérales, Randomisation dans les 24 h après le début des symptômes ou après le dernier moment où le patient est considéré comme normal (IC pendant le sommeil), Après imagerie cérébrale (TDM ou IRM).
Critères d’exclusion : Indication de fibrinolyse ou thrombectomie, Indication autre de double traitement anti-plaquettaire (stent coronaire, carotide). Indication d’anticoagulation, Hypersensibilité au TCG ou à l’ASA, Suspicion d’étiologie cardio-embolique, Indication de chirurgie carotidienne avec arrêt du traitement dans les 3 jours après randomisation, Présence d’un risque hémorragique connu, ATCD de complication hémorragique (intracérébrale, digestive) dans les 6 mois, Chirurgie majeure dans le mois avant randomisation.
|
|
Intervention |
Aspirine dose de charge 300 – 325 mg J1, puis 75 – 100 mg / J Ticagrelor dose de charge 180 mg, puis 90 mg x 2 / J pendant 30 à 34 J Puis Standard of Care.
|
|
Contrôle |
Aspirine dose de charge 300 – 325 mg J1, puis 75 – 100 mg / J Placebo du ticagrelor pendant 30 à 34 J. Puis Standard of Care.
|
|
Evaluation |
Critère primaire d’efficacité (composite) : premier AVC (Ischémique, hémorragique), décès toutes causes à 30 J. Critère secondaire d’efficacité : IC, dépendance selon le score de Rankin modifié (mRS) > 1 à 30 – 34 J, Critère primaire de sécurité (composite) : Premier événement hémorragique selon les critères GUSTO, Critères secondaires de sécurité : Hémorragies intracrâniennes (HIC) ou fatales, hémorragies modérées à sévères, évènements indésirables suffisamment graves pour entrainer l’arrêt du traitement.
|
|
Durée |
60 (+ 4) jours Suivi : V1 inclusion, V2 à 7 (+/- 2) J, V3 à 30 (+ 4) J, V4 à 60 (+ 4) J.
|
|
Notes |
Essai financé par AstraZeneca qui a fourni le ticagrelor et le placebo. Comité indépendant de surveillance de toutes les données.
|
RESULTATS
Onze mille soixante-treize patients sont enrôlés entre le 22 janvier 2018 et le 7 octobre 2019, 11 016 ont été randomisés (5 523 sous TCG, 5 493 sous placebo). Quinze patients ont retirés leur consentement dont 13 pendant la période de traitement. Un patient est perdu de vue, 0,2 % des patients ont un suivi incomplet pour le critère primaire et les données sur la dépendance sont manquantes pour 2,7 % des patients (Figure 1).
Figure 1 : Inclusions, randomisation et traitement.
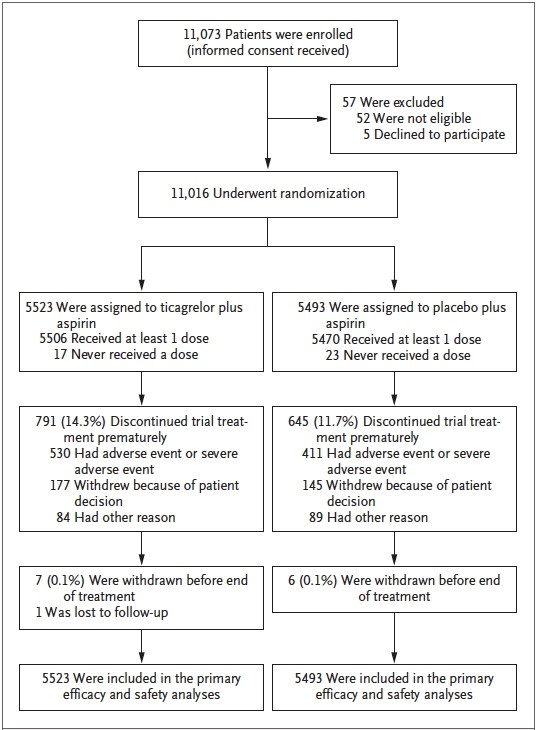
Les caractéristiques de base sont similaires dans les 2 groupes. Quatre-vingt-onze pour cents sont des IC et 9 % des AIT, moyenne d’âge 65 ans, 39 % de Femmes. Trente pour cents prenaient de l’aspirine avant l’événement index. Durant la période de traitement, 74 % des patients recevaient un traitement antihypertenseur, 83 % une statine, 28 % un hypoglycémiant (Tableau 1).
Tableau 1 : Caractéristiques cliniques des patients à l’inclusion.
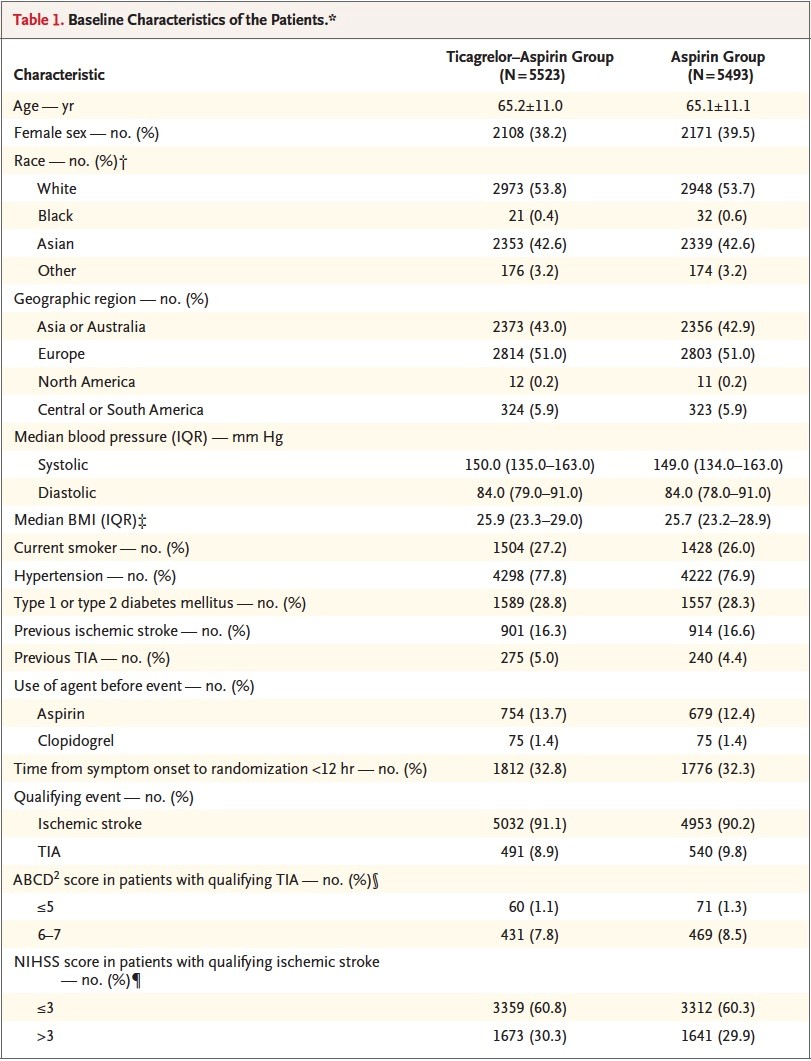
En ce qui concerne les critères d’efficacité : l’événement principal est survenu chez 303 patients sous TCG – ASA (5,5 %) et chez 362 patients sous ASA seule (6,6 %), HR = 0,83 (0,71 – 0,96, p = 0,02) (Figure 2). Le premier événement secondaire (IC) est survenu chez 276 patients sous TCG – ASA (5,0 %) et chez 345 patients sous ASA seule (6,3 %), HR = 0,79 (0,68 – 0,93, p = 0,004) (Tableau 2). Pour le second événement secondaire (dépendance selon le mRS), pas de différence significative entre les 2 groupes (23,8 % TCG – ASA, 24,1 % ASA seule). Une analyse de sensibilité tenant compte des données perdues ne modifie pas les résultats.
Figure 2 : Incidence cumulée du critère primaire d’efficacité.
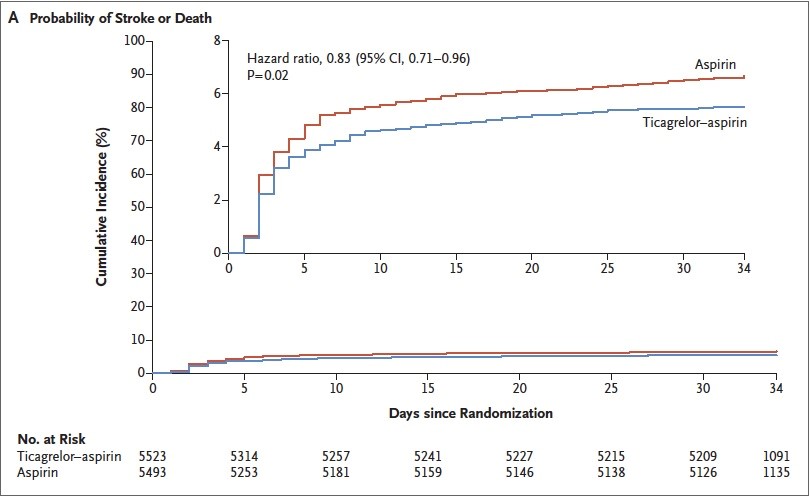
Tableau 2 : Critères d’efficacité et de sécurité.
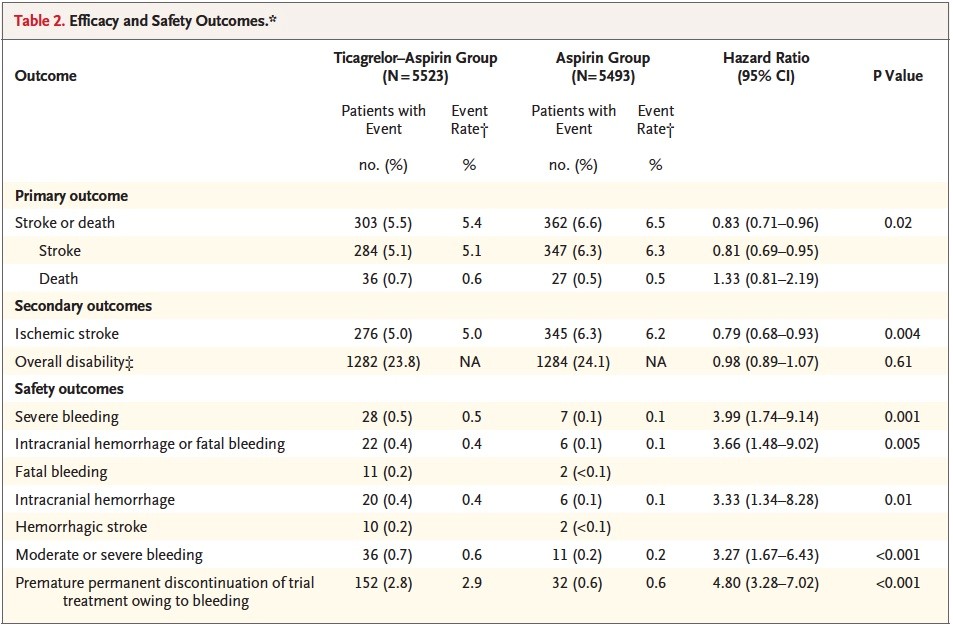
En ce qui concerne les critères de sécurité : l’événement principal (saignement sévère selon la classification GUSTO) est survenu chez 28 patients (0,5 %) sous TCG – ASA et chez 7 patients (0,1 %) sous ASA seule, HR = 3,99 (1,74 – 9,14, p = 0,001) (Figure 3).
Figure 3 : Incidence cumulée du critère primaire de sécurité.
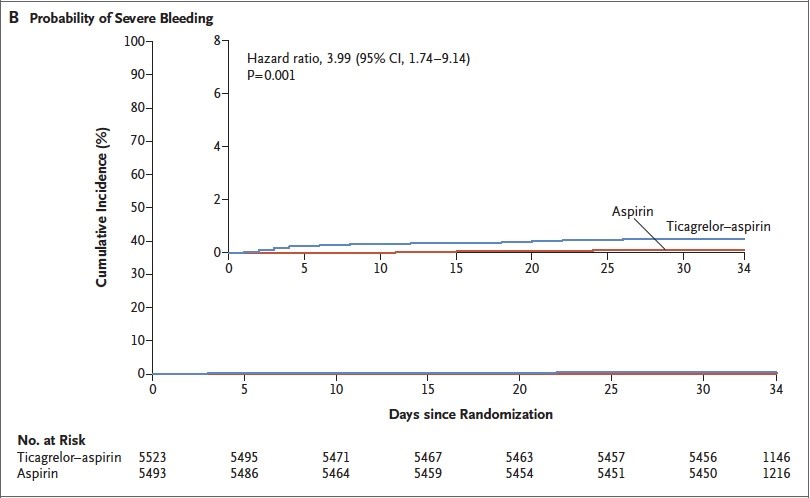
Le critère composite (HIC et hémorragies fatales) est survenu chez 22 patients sous TCG – ASA (0,4 %) et 6 patients sous ASA Seule (0,1 %). Les HIC sont survenues chez 20 patients sous TCG – ASA (0,4 %) et 6 patients sous ASA seule (0,1 %), une hémorragie fatale est survenue chez 11 patients sous TCG – ASA (0,2 %) et 2 patients sous ASA seule (< 0,1 %).
L’arrêt prolongé du traitement pour saignement est survenu chez 152 patients sous TCG – ASA (2,8 %) et chez 32 patients sous ASA seule (0,6 %).
DISCUSSION
Dans cet essai randomisé international, les patients ayant présenté un IC mineur (NIHSS ≤ 5) ou un AIT à haut risque ayant reçu dans les 24 h un traitement par TCG – ASA ont eu un meilleur pronostic en termes de récidive d’AVC et de décès que les patients qui n’ont reçu qu’un traitement par ASA seule à 30 jours. Ce bénéfice est également retrouvé pour le taux de récidive d’IC. Pas contre, aucun bénéfice n’est observé pour ce qui est du score de dépendance selon le mRS. L’association TCG – ASA est associée à un risque supérieur d’hémorragie sévère ou d’hémorragie cérébrale par rapport à l’ASA seule. L’association TCG – ASA permet d’éviter un événement du critère primaire d’efficacité pour 92 patients traités, au détriment d’un accident hémorragique sévère pour 263 patients traités.
Ces résultats sont comparables à ceux des études POINT et CHANCE qui comparaient l’association Clopidogrel – ASA à l’ASA seule.
|
Critère principal |
Clop – ASA |
ASA |
Inclusion |
Durée |
|
POINT |
5,0 % |
6,5 % |
12 h |
90 J |
|
CHANCE |
8,2 % |
11,7 % |
24 h |
Dual 21 J, mono 22 – 90 J |
La généralisation des résultats est limitée par l’exclusion des IC plus sévères (NIHSS > 5), des IC cardio-emboliques, d’une mise en route du traitement au delà de 24 premières heures et des indications de fibrinolyse / thrombectomie.
THALES et POINT font état d’une augmentation des hémorragies sévères, même si leur nombre est faible, contrairement à CHANCE.
CONCLUSION
Dans une population d’IC mineurs et d’AIT à haut risque, le risque d’AVC ou de décès est plus faible avec une association TCG – ASA qu’avec l’ASA seule sur une durée de traitement de 30 J. En revanche, aucune différence n’est retrouvée pour le score de dépendance et le risque d’hémorragie sévère est plus élevé.
Editorial P.M. Rothwell
Traitement anti-plaquettaire en prévention des récidives précoces d’AVC.
Rothwell PM. Antiplatelet Treatment to Prevent Early Recurrent Stroke. N Engl J Med. 2020;383(3):276-278.
Sans traitement urgent, le risque d’AVC majeur une semaine après un AIT ou IC mineur peut atteindre les 10 %. Plusieurs études ont montré qu’un traitement médical immédiat avec anti-plaquettaires, statines ainsi qu’un contrôle tensionnel réduisait le risque de 70 à 80 %, avec un bénéficie essentiellement attribuable à l’ASA ; malgré cela, il persiste un risque résiduel à 7 jours de 2 à 3 %. Compte tenu de l’efficacité de l’ASA, un traitement anti-plaquettaire plus intensif, soit avec une autre molécule soit par une association de 2 anti-plaquettaires, pourrait-il réduire ce risque résiduel ?
Aucun autre anti-plaquettaire utilisé seul n’a montré de supériorité franche par rapport à l’ASA en phase aigüe après IC mineur ou AIT. Le dipyridamole et le cilostazol apparaissent moins efficaces que l’ASA. Le ticagrelor est fréquemment utilisé en prévention des évènements thrombotiques coronariens, mais il est moins bien documenté en prévention secondaire des IC mineurs et AIT. L’étude SOCRATES, qui a comparé directement le TCG à l’ASA à la phase aigüe d’un IC mineur ou AIT à haut risque, a permis de mettre en évidence une réduction d’un critère secondaire (récidive précoce d’IC), particulièrement en cas d’instauration dans les 12 h après les premiers symptômes cliniques, sans augmentation du risque d’hémorragie cérébrale ou de saignement majeur. Cependant, l’étude a échoué à montrer une réduction significative du critère primaire composite (survenue d’AVC, d’IDM ou décès).
L’ASA reste le traitement anti-plaquettaire standard en cas d’AIT ou d’IC mineur, mais d’autres molécules peuvent être associées pour les patients à haut risque. Bien que l’association de l’ASA au dipyridamole ait montré un bénéfice par rapport à l’ASA seule pour la prévention des récidives précoces d’IC, l’association du clopidogrel à l’ASA s’est avérée plus efficace que l’ASA seule, mais avec un risque accru de saignement extra-crânien. L’extension de cette approche à une triple thérapie associant le dipyridamole, l’ASA et le clopidogrel (étude TARDIS) a entrainé un excès de saignements.
Deux comparaisons de double thérapie qui restaient non testées dans cette population étaient ASA + TCG versus ASA seule, et ASA + TCG versus ASA + clopidogrel. Johnston et coll. ont rapporté une comparaison chez plus de 11 000 patients avec AIT ou IC mineur avec ASA + TCG en prévention des AVC et des décès (THALES). Dans cette étude randomisée, double aveugle, les patients ayant présenté un IC non cardio-embolique ou un AIT à haut risque, et pour lesquels l’indication de fibrinolyse / thrombectomie n’était pas retenue, ont été assignés dans les 24 h après les premiers symptômes à un traitement par ASA + TCG ou ASA + placebo pendant 30 J. Le critère principal d’efficacité (récidive précoce d’AVC ou décès) est survenu chez 303 patients du bras ASA + TCG (5,5 %) et chez 362 patients du bras ASA + placebo (6,6 %), HR = 0,83 (0,71 – 0,96, p = 0,02). La différence est soutenue par une incidence plus faible des IC dans le bras ASA + TCG (276 vs 345 patients), HR = 0,79 (0,68 – 0,93, p = 0,004). Cependant, la double thérapie est associée à un haut risque d’hémorragies sévères (28 vs 7 patients, p = 0,001) et il n’y a eu aucun effet significatif sur la dépendance ou le décès.
Est-ce que les cliniciens choisiront maintenant le ticagrelor ou le clopidogrel s’ils veulent ajouter un second anti-plaquettaire à l’ASA ? Dans un autre essai, ASA + TCG fut plus efficace que ASA + Clopidogrel dans la réduction du risque d’évènements vasculaires ou décès à 1 an après un syndrome coronarien aigu. Quoi qu’il en soit, les résultats d'une comparaison directe de stratégies basées sur des traitements par double anti-plaquettaire chez les patients atteints d'AIT ou d'IC mineur sont en cours (CHANCE II), et les comparaisons indirectes ne sont pas fiables.
En dépit de ces mises en garde, il convient de noter que les données de l'essai en cours (CHANCE II) et de deux autres essais (CHANCE et POINT) pourraient légèrement favoriser le clopidogrel chez les patients présentant un AIT ou un IC mineur à la phase aigüe. Premièrement, dans POINT et CHANCE, les réductions relatives du risque de récidive d’IC avec ASA + clopidogrel avaient tendance à être plus importantes que la réduction avec ASA + TCG dans THALES. Deuxièmement, l'augmentation relative du risque de saignement majeur avec ASA + TCG était supérieure à celle avec ASA + Clopidogrel, en particulier en ce qui concerne les hémorragies intra-crâniennes. Un autre essai comparant directement ASA + TCG à ASA + clopidogrel en cas de syndrome coronarien aigu a également montré un risque plus élevé d'hémorragies intra-crâniennes avec ASA + TCG. Troisièmement, ASA + clopidogrel était associée à un risque global plus faible d’AVC invalidant ou mortel que ASA seule dans une analyse groupée des essais POINT et CHANCE, mais ce résultat n'était pas significatif avec ASA + TCG dans THALES. Les dispositions de ces déclarations provisoires incluent l'utilisation d'une dose de charge d'ASA plus élevée (300 à 325 mg) dans THALES que dans les essais sur ASA + clopidogrel (75,0 à 162,5 mg), et l'absence de notification (jusqu'à présent) des résultats dans le sous-groupe de patients de l'essai THALES présentant des événements dus à une athérosclérose des grosses artères, pour lesquels le TCG s'est avéré particulièrement efficace par rapport à l'ASA seule.
Enfin, les essais sus-mentionnés n'ont recruté qu'un sous-groupe à haut risque de patients atteints d'AIT, dont seuls ceux de la catégorie à risque le plus élevé ont bénéficié d'un double traitement anti-plaquettaire. Cette catégorie à haut risque a été déterminée selon le score ABCD2 (score de risque composite d'IC après AIT) de 6 ou plus (de 0 à 7, avec un risque plus important d'IC pour les scores les plus élevés). Le risque hémorragique associé à ASA + TCG pourrait dépasser le bénéfice pour les AIT à faible risque qui constituent la majorité des cas en pratique courante, et les résultats de cet essai ne doivent donc pas être sur-généralisés. Quelle que soit la combinaison d'anti-plaquettaires qui est privilégiée pour la minorité à haut risque, tous les patients doivent recevoir de l'ASA immédiatement après l'AIT, à moins que l'ASA ne soit contre-indiquée. Trop de patients sont renvoyés chez eux des services d'urgence sans ce traitement simple qui réduit considérablement le risque et la gravité d'une récidive précoce d’IC.
COMMENTAIRE
La précocité de la mise en route du traitement anti-plaquettaire par ASA (en association avec une statine) reste la recommandation majeure pour réduire le risque de récidive d’IC précoce. Les patients considérés à haut risque de récidive précoce peuvent bénéficier d’une double anti-agrégation plaquettaire ; le ticagrelor en association avec l’ASA n’a pas apporté de bénéfice majeur sur le risque de récidive précoce, au prix d’un risque de saignement accru (balance B/R en réduction de risque absolue : 1,1 – 0,3 = 0,8 %) face à l’ASA seule (THALES), et encore moins face à l’association ASA + clopidogrel (CHANCE, POINT). A l’heure actuelle, le clopidogrel reste le meilleur choix comme 2ème anti-plaquettaire dans l’attente de CHANCE II. La durée de traitement est également un élément important de la prise en charge ; elle reste pour l’instant sans réponse claire : 21 J pour CHANCE, 30 J pour THALES, 90 J pour POINT.
