Efficacité et sécurité de l’alirocumab après syndrome coronaire aigu en fonction du taux de LDL-C obtenu. Une analyse par score de propension de l’étude ODYSSEY.
« Le mieux est-il l’ennemi du bien ? »
En 1985, les prix Nobel Brown et Goldstein avaient suggéré une concentration physiologique de LDL-C chez l’homme entre 25 et 60 mg/dL. Cette concentration est de fait présente à la naissance et dans les populations de chasseurs-cueilleurs qui ont une très faible prévalence de maladies cardiovasculaires. Par contraste, la concentration moyenne de LDL-C parmi les adultes américains est de 120 mg/dL, avec une prévalence élevée d’évènements cardiovasculaires majeurs (ECVm).
Une question non résolue et importante est de déterminer quelle concentration de LDL-C est optimale pour réduire les ECVm avec une sécurité acceptable. Les études avec les statines ont montré que « The lower, the better », avec des taux de LDL-C obtenus entre 30 et 50 mg/dL, tandis que les inhibiteurs de PCSK9 permettent d’obtenir des taux encore plus bas. L’étude FOURIER avait montré que la réduction des ECVm était progressive avec la baisse du LDL-C sous evolocumab chez des patients déjà sous statines, jusqu’à des taux de LDL-C < 20 mg/dL. L’ESC avait ainsi recommandé des cibles de LDL-C < 55 mg/dL pour les patients à très haut risque cardiovasculaire et < 40 mg/dL en cas de récidive d’ECVm dans les 2 années précédentes.
Il subsiste néanmoins quelques limites d’interprétations de ces études :
1/ des différences de caractéristiques des patients en fonction des taux de LDL-C obtenus (notamment les taux initiaux de LDL-C) ;
2/ les taux de LDL-C mesurés directement ou calculés intègrent le cholestérol contenu dans la Lp(a) ; des taux élevés de LDL-C peuvent être liés à un taux élevé de Lp(a), qui n’est pas réduite par les statines ou l’ézétimibe ;
3/ des taux bas de LDL-C peuvent refléter l’adhésion du patient au traitement, et donc potentiellement son adhérence aux autres traitements.
Pour surmonter ces limites, les auteurs ont réalisé une analyse des données pré-spécifiées de l’essai ODYSSEY, et ont comparé les patients en trois strates selon le taux de LDL-C obtenu. A cette fin, ils ont utilisé le score de propension pour apparier les patients traités par alirocumab avec les patients du groupe placebo ayant des caractéristiques initiales et une adhésion au traitement identiques.
METHODES
ODYSSEY était un essai international randomisé, en double aveugle, contre-placebo, comparant l’alirocumab et le placebo (75 mg ou placebo en injection sous-cutanée toutes les 2 semaines) chez 18924 patients hospitalisés pour syndrome coronaire aigu (SCA) entre 1 et 12 mois avant la randomisation. Les patients inclus étaient déjà traités avec une statine de haute intensité (atorvastatine 40 ou 80 mg/j ou rosuvastatine 20 à 40 mg/j), avec au moins 1 des critères suivants : LDL-C ≥ 70 mg/dL, non-HDL-C ≥ 100 mg/dL ou apoB ≥ 80 mg/dL. Le LDL-C était calculé selon la formule de Friedewald et mesuré directement en cas de LDL-C calculé < 15 mg/dL ou de TG ≥ 400 mg/dL. La dose d’alirocumab était modulée en fonction du taux de LDL-C, avec une cible entre 25 et 50 mg/dL. En particulier, si le LDL-C était < 15 mg/dL sur deux prélèvements consécutifs, l’alirocumab était remplacé par le placebo pour le restant de l’étude. Le critère de jugement principal était composite : décès coronaire, IDM non fatal, hospitalisation pour angor instable, AVC ischémique fatal ou non.
Les patients inclus dans l’analyse étaient ceux qui n’avaient pas remplis le critère composite au 4ème mois de l’étude, date qui correspondait au nadir du taux de LDL-C sous alirocumab (soit 97.7% de la population en intention de traiter).
Les patients étaient classés en fonction du taux de LDL-C à 4 mois : > 50 mg/dL (n=2197), 25 à 50 mg/dL (n=3692) ou < 25 mg/dL (n=3357). Le score de propension étaient utilisés pour apparier chaque patient du groupe alirocumab avec un patient du groupe placebo ayant des caractéristiques initiales (y compris le taux de Lp(a)) et une adhésion au traitement identiques. L’adhésion au traitement était évaluée par le nombre d’injections réalisées au cours des 4 premiers mois de l’étude.
Des analyses de sensibilité étaient réalisées sur les patients du groupe alirocumab qui n’avaient pas eu de modification de dose après le 4ème mois et les patients dont le suivi était supérieur ou égal à 3 années. Une analyse de la relation entre les ECVm et la moyenne glissante des taux de LDL-C était également réalisée pour les patients du groupe alirocumab.
Le score de propension était utilisé pour évaluer la sécurité (effets indésirables : neuro-cognitifs, AVC hémorragique, diabète de novo) du traitement lorsque 2 taux de LDL-C consécutifs < 15 mg/dL étaient constatés chez les patients sous alirocumab, appariés avec les patients du groupe placebo ayant des caractéristiques initiales identiques (1 :3). A noter qu’il n’avait pas été retrouvé dans l’essai ODYSSEY d’effets indésirables de ce type avec l’alirocumab en comparaison avec le placebo.
RESULTATS
Un total de 18924 patients a été inclus dans 1315 sites de 57 pays. Le risque d’ECVm était réduit de 15% (HR 0.85 [0.78-0.93]) de même que les décès (HR 0.85 [0.73-0.98]) sur un suivi moyen de 2.8 années.
Dans le groupe alirocumab, comme attendu, il y avait une différence significative entre les taux moyens de LDL-C initial dans les strates > 50, 25 à 50 et < 25 mg/dL : respectivement 99, 88 et 79 mg/dL.
La Lp(a) était également plus élevée dans les strates > 50 mg/dL et 20 à 50 mg/dL (respectivement 26 et 27 mg/dL) que dans la strate < 25 mg/dL (15 mg/dL).
L’observance du traitement était significativement moins élevée dans la strate > 50 mg/dL (77.2% des patients avaient reçus au moins 4 doses) que dans les strates 25 à 50 mg/dL et < 25 mg/dL (respectivement 97.3%, 95.3% p<0.001).
A 4 mois, le taux moyen de LDL-C était de 31 mg/L dans le groupe alirocumab et de 87 mg/L dans le groupe placebo. Les taux moyens de LDL-C était de 72, 34 et 18 mg/dL dans les strates > 50, 25 à 50 et < 25 mg/L, soit des baisses respectives 27, 54 et 61 mg/L.
La figure 1 (à gauche en rouge) montre la courbe de modification des taux de LDL-C sous alirocumab entre 0 et 4 mois en fonction des taux atteints à 4 mois. Dans les strates < 25 et 25 à 50 mg/dL, presque tous les patients ont vus leur taux de LDL-C baisser, et d’au moins 50% chez respectivement 91.3 et 81.3% des patients, contre seulement 18.3% dans la strate > 50mg/dL ; cette différence était associée à la moins bonne observance du traitement. En bleu, figurent les modifications de LDL-C dans le groupe placebo : il y avait autant de patients qui augmentaient leur taux de LDL-C que de patients qui le diminuaient (avec des variations moyennes de 1%, 0% et 2% dans les strates > 50, 25 à 50 et < 25mg/dL).
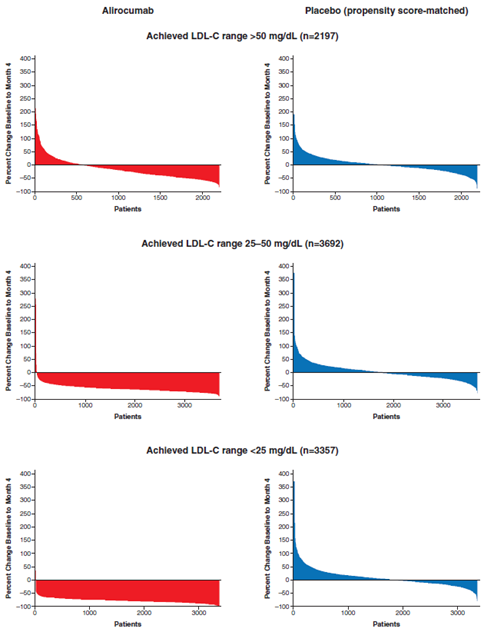
Figure 1 : Courbes de modifications des taux de LDL-C sous alirocumab (rouge) et placebo (bleu) entre 0 et 4 mois en fonction des taux atteints à 4 mois.
Les 1577 ECVm colligés après le 4ème mois représentaient 80.7% de la population en intention de traiter.
Le taux d’ECVm après 4 mois était de 3.92/100 patients-années (IC 3.66-4.19) dans le groupe placebo vs 3.16 (IC 2.94-3.41) dans le groupe alirocumab (HR 0.81 [0.73-0.89]), soit une réduction absolue de risque (RRA) de 0.75/100 patients-années.
Dans les différentes strates, les HR et RRA respectifs pour les ECVM étaient similaires :
×
> 50 : HR 0.87 (0.73-1.04), RRA = 0.62/100 patients-années
×
25 à 50 : HR 0.74 (0.64-0.87), RRA = 1.05/100 patients-années
×
< 25 : HR 0.74 (0.62-0.89), RRA = 0.92/100 patients-années
Pour les décès :
×
> 50 : HR 0.98 (0.74-1.29)
×
25 à 50 : HR 0.82 (0.64-1.06)
×
< 25 : HR 0.84 (0.64-1.10)
Analyses additionnelles
Parmi les 9462 patients du groupe alirocumab, 822 ont eu des modifications pré-spécifiées de dose après le 4ème mois. Chez les patients dont les doses n’avaient pas été modifiées, les taux d’incidence des ECVm étaient similaires à ceux de la première analyse.
Parmi les patients ayant au moins 3 ans de suivi (n = 8011), les résultats étaient également similaires.
L’analyse de la relation entre la réduction des ECVm et la moyenne glissante des taux de LDL-C pour les patients du groupe alirocumab, avec le taux de 50 mg/dL comme point de référence, montre une relation relativement linéaire au-delà de 25 mg/dL (LDL-C à 4 mois), mais une diminution de la réduction du risque en deçà de 23 mg/dL (avec un intervalle de confiance très large en dessus de 20 mg/dL) (figure 2).
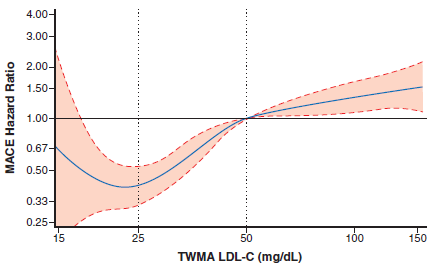
Figure 2 : Relation entre la réduction des ECVM et la moyenne glissante des taux de LDL-C pour les patients du groupe alirocumab.
Sécurité
Parmi les patients (n = 730) avec deux taux consécutifs de LDL-C < 15 mg/dL (pendant 6.8 mois en moyenne) et qui ont été placés sous placebo (8.3 mois en moyenne après randomisation), le taux moyen de LDL-C à 4 mois était de 16 mg/dL. Ces patients n’ont pas eu plus de troubles neuro-cognitifs ou d’AVC hémorragiques que les patients appariés du groupe placebo (n = 2152).
Parmi les 6769 patients non diabétiques sous alirocumab, 525 (7.8%) ont eu deux taux consécutifs de LDL-C < 15 mg/dL et n’avaient pas plus de diabète de novo que les 1675 patients appariés du groupe placebo (HR 1.10 [0.85-1.43], p = 0.46).
DISCUSSION
En résumé, les patients du groupe alirocumab dont le taux de LDL-C à 4 mois < 25 mg/dL ont une réduction de risque d’ECVm relative et absolue similaire aux patients avec un LDL-C entre 25 et 50 mg/dL. Des résultats identiques sont retrouvés pour les patients dont les doses d’alirocumab n’ont pas été adaptées au cours du suivi et chez ceux qui avaient un suivi dans l’étude de plus de 3 ans. L’analyse de la relation entre la réduction des ECVm et la moyenne glissante des taux de LDL-C suggère un nadir du risque d’ECVm pour un taux de LDL-C de 23 mg/dL. Les patients qui ont un taux de LDL-C > 50 mg/dL, plus faible qu’attendu, ont une moins bonne observance du traitement. Si l’étude ne montre pas de sur-risque neurocognitif ou hémorragique cérébral chez les patients avec un LDL-C < 15 mg/dL, il faut souligner la durée limitée de traitement de ces patients (6.8 mois).
Des études épidémiologiques et génétiques ont montré qu’un taux faible de LDL-C, situé dans la norme physiologique, est associé à un faible risque d’évènements coronaires. Les études sur les statines ont également bien démontré que la réduction de taux élevés de LDL-C permettait de réduire les ECVm en prévention secondaire et primaire. En revanche, la zone optimale de LDL-C sous traitement hypolipémiant pour réduire les ECV n’est pas encore définie. Avant l’ère des anti-PCK9, peu de patients avaient des taux de LDL < 25 mg/dL. Si l’assertion « The lower, the better » est prônée, aller au-delà des normes physiologiques peut ne pas être synonyme d’effets bénéfiques. Par ailleurs, l’association de faibles taux de LDL-C à un faible risque cardiovasculaire peut être également liée à de faibles taux de LDL-C et de Lp(a) de base et tout le long de la vie, ou à une bonne adhésion au traitement hypolipémiant et par extension à tous les autres traitements et aux règles d’hygiène de vie.
Une analyse secondaire des données pré-spécifiées de l’essai FOURIER (evolocumab vs placebo) avait précédemment été conduite par Giugliano et al. (1) et avait montré, suivi un suivi moyen de 2.2 années, une relation quasi-linéaire entre le taux de LDL-C obtenu à 4 semaines et la survenue d’ECVm, jusqu’à des taux de LDL-C de 0.2 mmoles/L (7.6 mg/dL). Mais l’ajustement était réalisé sur les variables initiales uniquement dans le groupe dont le taux de LDL-C était < 0.5 mmoles/L. et surtout ces variables n’incluaient pas le taux de Lp(a) ni l’observance du traitement.
S’appuyant sur les résultats de la Cholesterol Treatment Trialist qui avait montré une réduction de 22% des ECVm pour chaque réduction de 1 mmole/L du LDL-C, Schwartz et al ont calculé pour chaque strate de LDL-C obtenu (> 50, 25 à 50 et < 25 mg/dL) les Hazard Ratios de réduction de risque (respectivement 0.84, 0.73 et 0.73), et souligné la quasi-correspondance avec les HR obtenus dans l’étude (0.87, 0.74 et 0.73).
Finalement, les résultats de l’étude sont en accord avec les recommandations de l’ESC citée en introduction et avec celles de l’AHA, dans lesquelles la prudence est de mise lorsque le taux de LDL-C est < 25 mg/dL.
Les auteurs relèvent des limites à l’étude :
- l’analyse de données après randomisation (taux de LDL obtenus) peut être source de facteurs de confusion résiduels ;
- les patients avec des taux de LDL-C < 25 mg/dl (à 4 mois) ne semblent pas avoir de réduction de risque d’ECVm supplémentaire par rapport aux patients de la strate 20-50 mg/dL, mais l’intervalle de confiance est très large.
- la durée de suivi relativement courte de l’étude ne préjuge pas de l’efficacité ni de la sécurité à plus long terme.
Les auteurs concluent que l’étude va dans le sens des recommandations ESC concernant le traitement hypolipémiant des patients à haut risque cardiovasculaire : un autre traitement doit être ajouté lorsque le LDL-C sous statines reste > 70 mg/dL, avec un objectif < 55 mg/dL, si possible < 40 mg/dL, mais pas nécessairement < 25 mg/dL.
COMMENTAIRES
Cette étude peut apparaitre finalement plutôt rassurante. Elle suggère qu’il ne faut peut-être pas dépasser certaines limites physiologiques, en l’occurrence ici la limite inférieure du taux de LDL-C que la nature nous permet d’observer : chez le nouveau-né et dans les populations vertueuses sur le plan de l’hygiène alimentaire. Elle nous suggère également, à travers l’écart type très large du risque d’ECVm dans la strate < 25 mg/dL, que nous sommes sans doute très différents quant à la sensibilité de notre paroi vasculaire au seul taux de LDL-cholestérol, illustrant la complexité de la prise en charge d’un patient en particulier. Elle nous rappelle aussi l’importance de l’observance du traitement. Les recommandations ESC 2019 sur les dyslipidémies précisaient les conditions d’une bonne acceptation du traitement par le patient : une attitude empathique du médecin, l’absence de jugement, une explication simple sur le traitement, l’utilisation d’image ou de vidéo, susciter les questions du patient, etc. Il faut reconnaître que de nos jours cette information est rendue particulièrement chronophage par l’impact délétère des médias. Une bonne observance passe également par la persévérance nécessaire, en cas de survenue d’un effet indésirable, pour mettre en évidence de façon certaine la relation de cause à effet, et ne pas attribuer au traitement la premier symptôme anormal allégué par le patient.
Références
1.
Giugliano RP, Pedersen TR, Park JG et al; FOURIER Investigators. Clinical efficacy and safety of achieving very low LDL-cholesterol concentrations with the PCSK9 inhibitor evolocumab: a prespecified secondary analysis of the FOURIER trial. Lancet. 2017 Oct 28;390(10106):1962-1971.
