Depuis la publication de plusieurs essais cliniques randomisés en 1995 et 2010, le traitement optimal de la maladie carotidienne asymptomatique a impliqué une intervention sélective.Depuis lors, la thérapie médicale a progressé et plusieurs rapports ont démontré de meilleurs résultats avec le traitement médical seul, soulevant des questions sur le bénéfice absolu supplémentaire de la chirurgie pour prévenir l'accident vasculaire cérébral (AVC) chez les patients asymptomatiques.
Le risque d'AVC d'une atteinte carotidienne asymptomatique sans revascularisation chirurgicale est difficile à déterminer car les sources de données ont été limitées à des groupes non chirurgicaux d'essais cliniques, à de rares études prospectives ou à de plus petites études basées sur la chirurgie.De plus, compte tenu de leur ancienneté, ces travaux ne tiennent pas compte des avancées récentes en matière de réduction du risque cardiovasculaire dans la population.
L'objectif de cette étude était de décrire le risque à long terme d'AVC chez les patients atteints de sténose carotidienne sévère asymptomatique qui ne sont pas opérés, dans une population communautaire plus contemporaine et ethniquement diversifiée.
METHODES
Projet approuvé par le comité institutionnel de revue de la Kaiser Permanente Northern California (KPNC) avec une dérogation spécifique au consentement pour une étude rétrospective de données uniquement. KPNC est un système de prestation de soins de santé intégré qui dessert plus de 4,5 millions de membres dans 21 centres médicaux et hôpitaux. La démographie du système de santé est comparable à celle de l'ensemble de la population de patients assurés de la région.
Assemblée de la cohorte de maladies
Les patients présentant une sténose carotidienne sévère (70 % à 99 % selon les critères de consensus de la Society of Radiologists in Ultrasound pour les études échographiques et les critères de l'essai nord-américain d'endartériectomie symptomatique carotidienne [NASCET] pour l'imagerie axiale) ont été identifiés de 2008 à 2012. Si 2 études ont été réalisées dans un court laps de temps et que les résultats étaient différents, l'étude en coupe axiale a généralement été utilisée pour définir la catégorie de sténose. Si 2 échographies ont été réalisées dans la même période, la seconde a été utilisée si elle était informative et distincte de la première. Si la catégorie de sténose de la deuxième échographie était inférieure à 70 %, cette artère était exclue de l'étude en cours. Pour stratifier une sous-catégorie de sténose de haut grade à la fois à l’inclusion et pendant le suivi, un seuil échographique de sténose de haut grade a été désigné par une vitesse systolique maximale de l'artère carotide interne de 350 cm/s ou plus ou une réduction en diamètre NASCET de 90 % à 99 % en imagerie axiale.
Les critères d'exclusion étaient les suivants : (1) patients sans adhésion active à un régime de santé pendant 1 an avant l'étude index ; (2) lésions non athéroscléreuses de l'artère carotide (par exemple, dissection, dysplasie fibromusculaire, traumatisme) ; (3) ATCD de revascularisation carotidienne homolatérale (endartériectomie ou stenting de l'artère carotide) à tout moment avant la quantification à l’inclusion ; et (4) accident vasculaire cérébral ou accident ischémique transitoire (codes de diagnostic ICD-9-CM et ICD-10-CM) dans les 6 mois précédant la mesure index. Un examen manuel des dossiers chirurgicaux, des notes cliniques et d'autres documents pertinents a été effectué pour confirmer la latéralité, le moment et la présence d'une lésion asymptomatique. Les artères éligibles ont été suivies jusqu'au 31 décembre 2019, avec censure au décès, désinscription de l'adhésion ou intervention carotide ipsilatérale.
Covariables
Les caractéristiques de base ont été collectées, y compris les données démographiques, les comorbidités pertinentes, les médicaments cardiovasculaires et les valeurs de la pression artérielle et les variables biologiques. Les valeurs obtenues les plus proches de la date de l'étude d'index ont été utilisées comme référence. Les origines ethniques, signalées par les patients lors de l'établissement des dossiers médicaux, ont été incluses pour aider les lecteurs à comprendre la diversité de la cohorte communautaire. Un indice de comorbidité préalablement assemblé en interne et en externea été utilisé comme score général d'ajustement au risque (comorbidity point score, version 2 [COPS2]) pour les patients, sur la base des codes de diagnostic et de la saisie automatisée des données physiologiques (1).
L'utilisation initiale de médicaments cardiovasculaires (p. ex., statines, antihypertenseurs) a été définie par au moins une ordonnance établie au cours des 12 mois précédant l'entrée dans l'étude. L'observance a été évaluée par le ratio de possession de médicaments (MPR) déterminé à partir des dossiers de pharmacie des patients externes. Le MPR de base a été calculé en divisant le nombre total de jours d'ordonnances ambulatoires délivrées au cours de l'année précédente par 365 jours. Au cours du suivi, ce calcul a été modifié pour inclure les jours fournis parmi tous les médicaments délivrés jusqu'à la fin du suivi pour chaque année d'étude comme numérateur et la durée maximale de suivi ou l'année d'étude comme dénominateur. Le MPR calculé était un pourcentage continu et, à des fins d'analyse dichotomique, un MPR supérieur à 80 % (MPR80) était défini comme adhérent.
Evènements
Le critère de jugement principal était défini comme un infarctus cérébral ipsilatéral à la lésion carotidienne. Chaque événement identifié a été examiné manuellement par un chirurgien vasculaire ou un neurologue spécialiste de l'AVC ; les désaccords ont été tranchés par consensus. Les compte-rendus d'imagerie disponibles (tomodensitométrie, imagerie par résonance magnétique), les compte-rendus de consultation de neurologie ou de chirurgie vasculaire et d'autres documents pertinents ont été examinés. Les accidents vasculaires cérébraux ont été confirmés, puis attribués à la latéralité, à l'emplacement et à l'étiologie avec les preuves cliniques appropriées. Les sous-types d'infarctus cérébraux ont été classés selon les critères publiés. Lorsque les données d'imagerie étaient informatives, la présence d'une lésion ischémique à l'imagerie diagnostique était comptabilisée comme un AVC, même si la durée des symptômes était inférieure à 24 heures. Malgré une approche multi-spécialisée de l'AVC, certains cas n'ont pas pu être définitivement tranchés, de sorte que ces cas ipsilatéraux ont été prudemment classés comme ayant satisfait le critère principal. Lors de l'arbitrage, s'il y avait un AVC lacunaire présumé ipsilatéral à la sténose carotidienne, il était jugé lié à la lésion carotidienne. De plus, les accidents vasculaires cérébraux d'étiologie inconnue ou d'étiologies multiples possibles qui étaient du même côté que la lésion carotidienne index ont été comptabilisés dans le critère principal. Les critères de jugement secondaires comprenaient la progression de la sténose vers un grade élevé ou une occlusion, la prescription de médicaments, l'observance du traitement, la pression artérielle, les taux de lipoprotéines de basse densité (LDL) et la mortalité toutes causes confondues.
Calcul de la taille de l'échantillon
En raison de la nature descriptive de cette étude, les calculs de la taille de l'échantillon n'ont pas été effectués et la taille de la cohorte a été fixée par les critères choisis. L'adéquation de la taille de l'échantillon a été évaluée par les intervalles de confiance autour des estimations centrales primaires.
Analyses statistiques
Les données manquantes, y compris la pression artérielle, la créatinine, les lipoprotéines de haute densité (HDL), les LDL, l'hématocrite, les triglycérides et l'indice de masse corporelle, ont été remplacées par les valeurs médianes des participants à l'étude corrigées en fonction du sexe. Ces caractéristiques ont été comparées entre le groupe « intervention asymptomatique » et le groupe « sans intervention » avec des tests χ2 ou de Fisher pour les variables catégorielles le cas échéant, et les variables continues ont été comparées entre les groupes à l'aide de tests t indépendants à 2 échantillons. Les scores COPS2 ont été comparés à l'aide du test Mann-Whitney U (Wilcoxon rank-sum).
En cas de sténose sévère asymptomatique bilatérale, chaque artère était analysée indépendamment de l'artère controlatérale. Les données brutes des résultats d'intérêt ont été calculées, la méthode des tables de mortalité (méthode indirecte sans groupe de comparaison) et les analyses de survie de Kaplan-Meier ont été effectuées pour l'AVC ipsilatéral. Nous avons également examiné le risque d'AVC tout en tenant compte des risques compétitifs de décès et d'intervention. Un modèle de risques compétitifs a été développé en utilisant une fonction d'incidence cumulative non paramétrique pour déterminer l'incidence cumulative de l'AVC ipsilatéral. En présence d'un événement compétitif tel que la mortalité, la fonction d'incidence cumulée dépendait du taux de risque de l'événement d'intérêt (AVC) ainsi que du taux de risque du ou des événements concurrents. La fonction d'incidence cumulée dans les risques compétitifs peut être estimée à l'aide de l'estimateur d'Aalen-Johansen. Ce modèle tient compte des événements compétitifs de décès et d'intervention pour déterminer l'incidence cumulée du résultat principal.
Un modèle de risques proportionnels de Cox a été utilisé pour identifier les facteurs de risque pour le résultat principal. Les covariables dans les analyses de régression ont été déterminées sur la base d'une association significative avec le résultat d'intérêt, ainsi que sur la pertinence clinique. Les variables incluses dans le modèle comprenaient l'âge, le sexe, la sténose de haut grade, les antécédents d'AVC controlatéral, le score COPS2, le diabète, l'utilisation et l'observance des anticoagulations ou des statines, ainsi que la pression artérielle, les taux de LDL, de HDL et de triglycérides. L'hypothèse des risques proportionnels pour les covariables du modèle de Cox a été évaluée sur la base des sommes cumulatives des résidus de martingale au cours du suivi et à l'aide de diagrammes de résidus de Schoenfeld mis à l'échelle. Alors que les tests des risques proportionnels étaient significatifs pour l'âge (P = 0,03), la sténose de haut grade (P = 0,02) et le HDL (P = 0,01), indiquant une non-proportionnalité, les graphiques résiduels de Schoenfeld pour ces variables n'indiquaient qu'une légère variation des rapports de risque (HR) au fil du temps. Étant donné que l'écart par rapport à l'hypothèse des risques proportionnels est faible pour ces variables, nous rapportons les HR estimés sous l'hypothèse des risques proportionnels et interprétons les estimations d'effet pour ces variables comme des HR moyens au cours du suivi.
Toutes les analyses ont été effectuées à l'aide de SAS 9.4 (SAS Institute Inc) avec le seuil de signification fixé à une valeur P bilatérale inférieure à 0,05. En raison du potentiel d'erreur de type I dû aux comparaisons multiples, les résultats des analyses des critères d'évaluation secondaires doivent être interprétés comme exploratoires.
RESULTATS
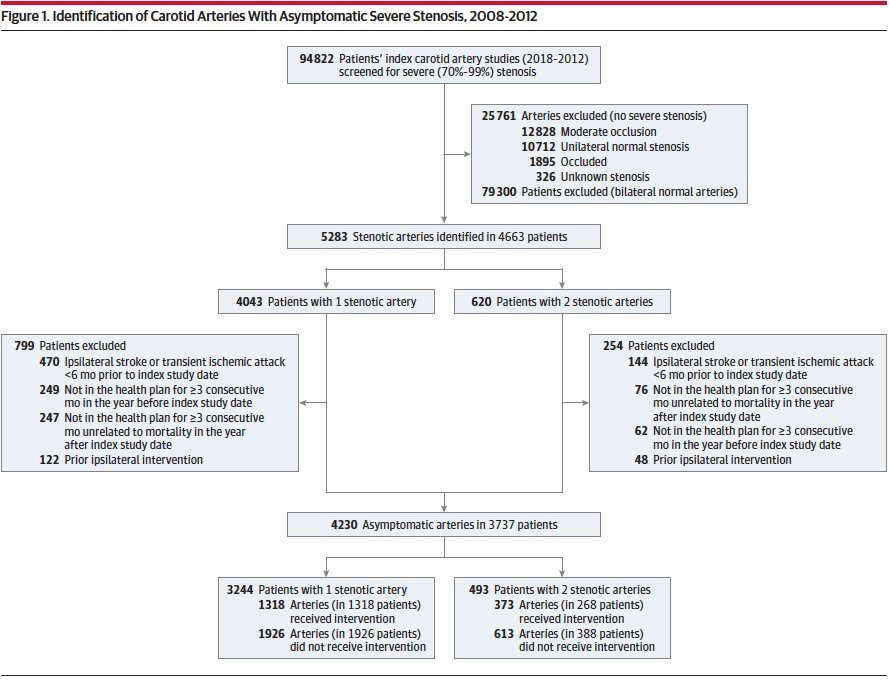
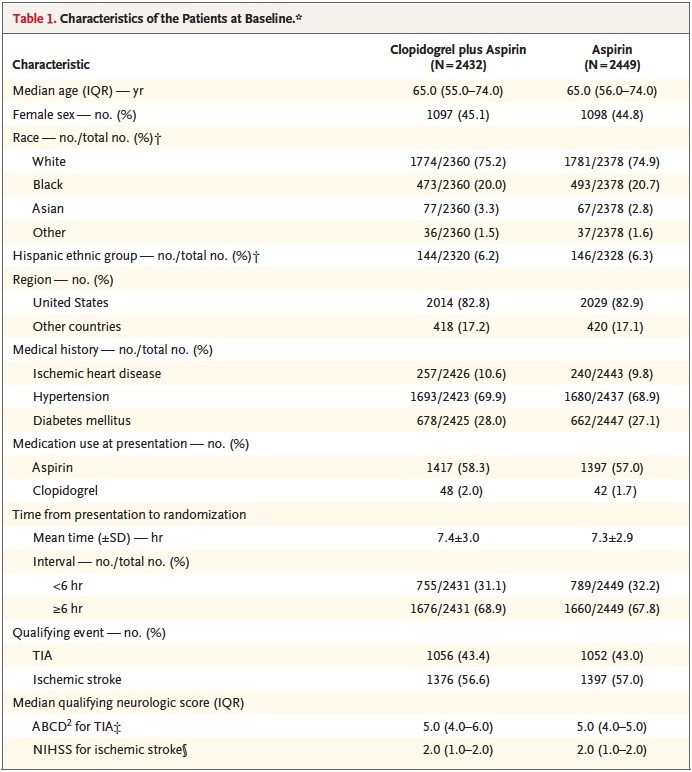
La figure 1 illustre l'assemblage de la cohorte. Au total, 4230 artères présentant une sténose sévère asymptomatique chez 3737 patients ont été incluses dans la cohorte finale. Les caractéristiques de base du groupe « chirurgical » sont décrites dans le tableau 1. En bref, les patients « non chirurgicaux » avaient tendance à être plus âgés, de sexe féminin et avec un niveau de comorbidité global plus important. L'âge moyen de la cohorte était de 73,8 ans (SD 9,5), 58,1 % étaient des hommes et 73,0 % étaient des Blancs. Sur les 3737 patients, 2314 patients avec 2539 artères incluses n'ont pas subi d'intervention avant la fin de l'étude. Parmi les patients ne répondant pas au critère d'évaluation principal ou subissant une intervention, 1553 (36,7%) patients sont décédés et 268 (6,3%) patients ont été désinscrits du plan de santé au cours de la période d'étude.
Critère principal : Infarctus Cérébral homolatéral à la sténose carotide
Il y a eu 133 Infarctus cérébraux liés à la carotide homolatérale chez 129 patients, avec un délai médian entre l'entrée dans l'étude et l'événement d'AVC de 24,8 mois (IQR, 7,9-46,5). Parmi les AVC signalés comme résultat principal, 3 cas étaient de nature lacunaire, 18 cas avaient plusieurs étiologies possibles et 13 cas n’avaient pas d’étiologie connue (AVC cryptogéniques). Le taux annuel brut (non ajusté) d'AVC ipsilatéral était de 0,9 % (IC 0,7-1,2). Parmi les 133 AVC homolatéraux, 35 patients (27,1 %) ont subi une intervention ultérieure et 86 (66,7 %) patients sont décédés (toutes causes confondues) dont 15 dans les 30 jours et 19 patients supplémentaires dans l'année suivant l'AVC. Il y avait 43 patients qui ont survécu à la période d'étude après un AVC. La survie médiane après un AVC ipsilatéral, y compris ceux bénéficiant d’une intervention, était de 25,3 mois (IQR 9,7-54,5).
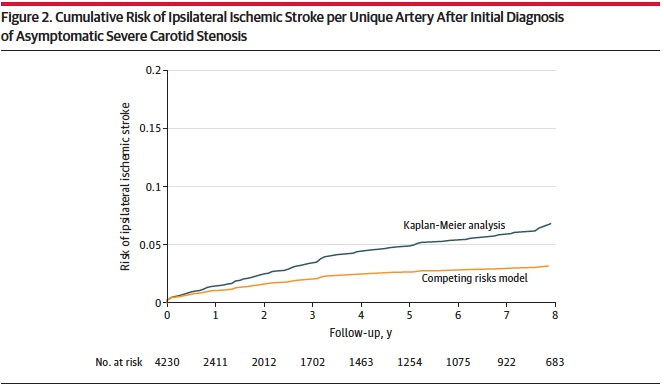
Les taux annuels moyens globaux non ajustés et le risque cumulé d'AVC sur 5 ans par type sont présentés dans le tableau 2. Le risque cumulé d'AVC lié à la carotide homolatérale à 5 ans dans l'analyse de Kaplan-Meier était de 4,7 % (IC à 95 %, 3,9 % à 5,7 %) (Figure 2) parmi les patients opérés, et il était de 4,1 % (IC à 95 %, 3,3 %-5,0 %) chez les patients non opérés. En tenant compte du risque compétitif de décès et d'intervention pour une pathologie asymptomatique, l'incidence cumulée d'AVC ipsilatéral était de 1,0 % (IC à 95 %, 0,8 % à 1,4 %) à 1 an et de 2,7 % (IC à 95 %, 2,2 % à 3,2 %) à 5 ans.
Dans l'analyse de régression de Cox multivariée, les variables indépendantes significatives associées à l'AVC ischémique ipsilatéral comprenaient l'âge (pour chaque augmentation sur 10 ans : RR ajusté, 1,25 [IC à 95 %, 1,02-1,53] ; P = 0,03), une lésion de haut grade à l’inclusion (HR ajusté, 1,73 [IC à 95 %, 1,06-2,84] ; P = 0,03) et un antécédent d'AVC non ipsilatéral (HR ajusté, 2,81 [IC à 95 %, 1,63-4,84] ; P < 0,001). L'utilisation de toute statine pendant le suivi de l'étude était associée à un risque réduit d'AVC (RR ajusté, 0,38 [IC à 95 %, 0,21-0,72] ; P = 0,003).
Critères secondaires
Sténose initiale et état de l'artère controlatérale
Parmi les 3 737 patients de la cohorte globale asymptomatique, 493 (13,2 %) présentaient une sténose carotidienne sévère bilatérale répondant aux critères de sélection. Sur les 4 230 artères, 473 (11,2 %) étaient considérées comme de haut grade à l’inclusion, 1 185 (28,0 %) présentaient une sténose modérée controlatérale, 1 002 (23,7 %) présentaient une sténose sévère controlatérale et 173 (4,1 %) présentaient une occlusion carotidienne controlatérale à l’inclusion.
Progression de la maladie carotidienne au cours du suivi
Parmi les 3078 artères qui ont subi 1 ou plusieurs imageries supplémentaires au cours du suivi, 1815 concernaient des patients non opérés. Parmi ces sténoses sévères mais non de haut grade, 391 (21,5 %) ont évolué vers un haut grade au cours du suivi et 153 (8,4 %) ont évolué vers une occlusion. Parmi 216 artères présentant une sténose de haut grade à l'inclusion et non opérées, 61 (28,2 %) ont évolué vers l'occlusion. Soixante-dix-sept des 133 AVC homolatéraux (57,9 %) étaient associés à une sténose initiale sévère sans progression, 32 (24,1 %) étaient associés à une progression vers une sténose de haut grade et 19 (14,3 %) étaient associés à une sténose initiale de haut grade. Sur les 163 artères (3,9 %) qui présentaient une occlusion carotidienne dans l’intervalle, 17 (12,8 % des 133 AVC liés à la carotide homolatérale) étaient associées à un AVC lié à la carotide homolatérale (10 avec une sténose sévère initiale ; 7 avec sténose initiale de haut grade).
Mortalité toutes causes confondues
Le taux non ajusté de mortalité toutes causes confondues était de 51,4 % (tableau 2) avec un taux brut annuel moyen de 13,6 % (IC à 95 %, 12,6 %-14,7 %) pendant la durée moyenne (ET) de suivi de 4,1 (3,6) années. L'analyse des tables de survie a fourni des probabilités cumulées non ajustées de décès toutes causes confondues à 1 an (9,9 % [IC à 95 %, 9,0 % - 10,9 %]) et à 5 ans (45,2 % [IC à 95 %, 43,4 % -46,9 %]).
Utilisation et observance des médicaments
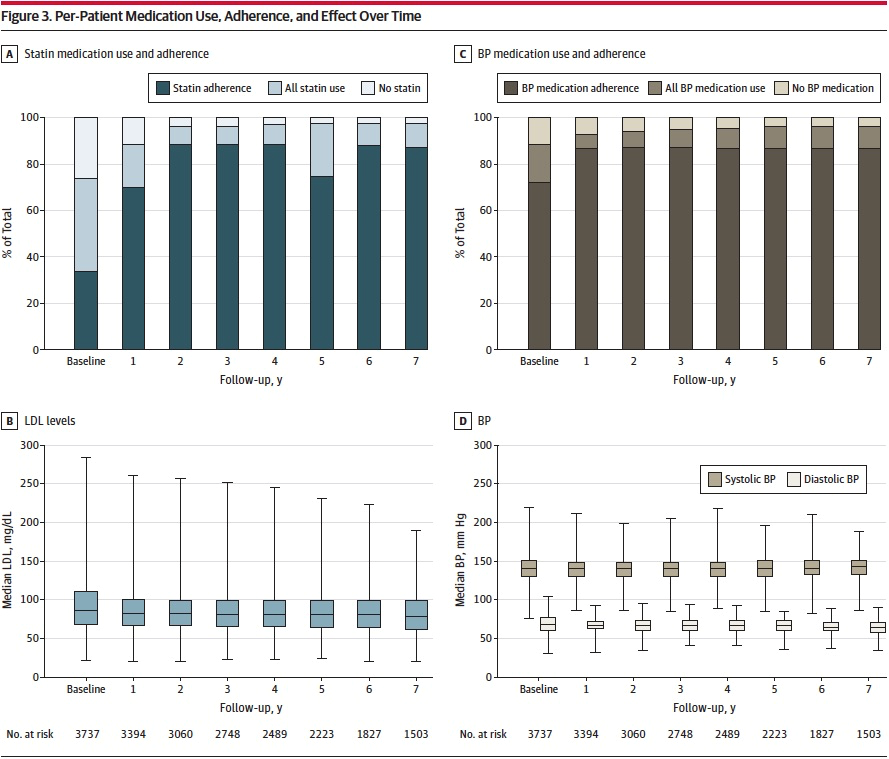
Les pressions artérielles médianes initiales de la cohorte (patients uniques) étaient de 130 mmHg (IQR, 120-140 mmHg) pour la systolique et de 68 mmHg (IQR, 60-76 mmHg) pour la diastolique, dont 71,8 % qui avaient au moins 1 tension artérielle de base inférieure à 140/90 mmHg. Le LDL-C médian initial était de 87 mg/dL (IQR, 72-108 mg/dL) et la prévalence du tabagisme actif chez les patients ayant des antécédents de tabagisme connus au départ était de 13,7 % (455/3319). Soixante-quatorze pour cent des patients (n = 2 768) se sont vu prescrire une statine au départ avec une adhésion initiale aux statines de 45,2 % au cours de l'année précédant l’inclusion. Au cours du suivi, toute utilisation de statines s'est améliorée à 91,1 %, l'adhésion aux statines augmentant à 70,7 %. Sur les 3 299 patients ayant reçu un médicament antihypertenseur prescrit au cours de l'année précédant l'entrée dans l'étude, 82,2 % (n = 2 711) ont démontré une adhésion au traitement initial. Sur les 3 526 patients qui se sont vu prescrire des médicaments antihypertenseurs au cours du suivi, 88,5 % (n = 3 120) ont démontré une observance thérapeutique. La figure 3 (panneaux A à D) montre des observations dépendant du temps sur l'utilisation annuelle des médicaments et l'observance de ces médicaments ainsi que les pressions artérielles et les niveaux de LDL mesurés associés. Comme le montrent ces figures, les deux indices semblaient être bien contrôlés et sont restés inférieurs aux niveaux cibles recommandés pendant la période d'étude.
DISCUSSION
Dans une cohorte communautaire de patients atteints de sténose carotidienne sévère asymptomatique qui n'ont pas bénéficié de la chirurgie, le taux estimé d’infarctus cérébral homolatéral à la sténose était inférieur aux données historiques. À notre connaissance, cette étude est l'évaluation la plus importante et la plus récente du risque d’infarctus cérébral ipsilatéral à long terme, et donne un aperçu des facteurs associés à l'AVC, dans un contexte de population à haut risque accompagné d’une mortalité importante.
De plus, cette étude donne un aperçu du risque réel d'AVC dans ce type de population, car le modèle de risques compétitifs utilisé dans l'analyse des résultats peut être plus précis qu'un modèle traditionnel à risques proportionnels, avec prise en compte du décès ou de la chirurgie carotidienne comme des événements concurrents plutôt que de censurer les patients décédés ou ayant subi une intervention au cours de la période de suivi. Cette différence est particulièrement pertinente dans une population de patients présentant de nombreuses comorbidités et un taux de mortalité élevé en conséquence. L'analyse de Kaplan-Meier des taux d'événements, plus couramment utilisée, traite le décès comme un événement censurant et suppose à tort que ceux qui sont censurés ont le même risque d'AVC que ceux qui ne le sont pas, surestimant ainsi l'incidence cumulée des AVC.
Les données sur les résultats du traitement médical moderne des maladies carotidiennes asymptomatiques sont rares. La plus grande étude prospective à cet égard était l'étude ACSRS (Asymptomatic Carotid Stenosis and Risk of Stroke), qui a recruté 1121 patients avec une sténose de 50 % à 99 % dans des centres non américains de 1998 à 2002. Cette Cohorte a recensé 130 évènements ipsilatéraux dont 59 étaient des accidents vasculaires cérébraux. De plus, l'étude a démontré une association entre la progression de la maladie et le risque d'accident vasculaire cérébral. Une critique de cette étude était le regroupement des sténoses entre 50 % et 99 %, car la pratique américaine conventionnelle et le conseil préopératoire sur les risques subdivisent cette catégorie selon les critères de la Society of Radiologists in Ultrasound. Dans l'étude actuelle, les critères d'inclusion spécifiaient une sténose de 70 % à 99 % pour être qualifié et entrer dans l'étude. La pratique actuelle est également sous tendue par les résultats du groupe chirurgie différée de l'essai ACST-1 (randomisation des patients de 1993 à 2003 avec une sténose de 60 % à 90 % pour un traitement chirurgical immédiat ou différé). Utilisant les courbes d’analyse de survie, cette étude a observé un risque de 10 % de tout AVC non péri-opératoire dans le groupe différé à 5 ans.
En revanche, il existe des rapports plus récents concernant la réduction du risque d'AVC. Une méta-analyse de 2009 a montré une baisse persistante du risque chez les patients asymptomatiques dans les études publiées après 1990 par rapport à l'ère des essais randomisés. La conclusion selon laquelle les effets de la thérapie médicale contemporaine étaient maintenant similaires aux effets de la chirurgie pour la réduction du risque d'AVC était controversée ; on s'est inquiété de l'inclusion des sténoses modérées dans le calcul du risque, ce qui a sans doute dilué le risque d'AVC.
L'étude actuelle rapporte le risque d'AVC dans une cohorte de sténoses carotidiennes pertinentes sur le plan chirurgical en utilisant des critères de consensus récents. Dans cette cohorte, la notification des AVC a été normalisée à l'échelle du système, ce qui a conduit à une haute fidélité dans la détection des événements pertinents. La prise en charge de l'AVC au KPNC est régionalisée et tous les cas sont confirmés à la fois sur la foi du dossier médical et de la facturation selon les recommandations de bonne pratique. De plus, la nature intégrée des dossiers de santé électroniques et le faible taux de désinscription ont permis un suivi complet et une évaluation des variables associées. Des méthodes libérales d’estimation des taux d'AVC ont été utilisées, y compris les AVC lacunaires inconnus probables lors du calcul des taux d'AVC ipsilatéraux, car il peut y avoir une incertitude quant à l'étiologie. Cette catégorie comprenait les patients sans imagerie cérébrale ou lorsque 2 étiologies ou plus étaient cliniquement possibles (p. ex., arythmie cardiaque et sténose carotidienne). Ainsi, le taux réel d'AVC dû à une maladie carotidienne peut être inférieur aux estimations présentées. La large représentation de la cohorte de l'étude et de la population KPNC en général implique que ces résultats peuvent être généralisables aux patients assurés dans une région géographique similaire aux États-Unis.
Il y avait plusieurs liens entre la progression de la sténose ou l'occlusion artérielle et l'incidence de l'AVC. La modélisation des risques proportionnels a montré qu'une lésion de haut grade au départ ou la progression d'une lésion vers une sténose ou une occlusion de haut grade était associée à un risque accru d'AVC. Bien que cette association n'ait pas été démontrée dans des essais cliniques randomisés, ces résultats font écho aux conclusions du rapport de l'ACSRS.L'implication de ces résultats suggère que la cohorte réelle de patients à risque plus élevé d’infarctus cérébral, et qui sont donc des candidats raisonnables pour une chirurgie, peut être beaucoup plus petite que celle que les normes actuelles nous dictent.
La conception de l'étude comprenait des variations en fonction du temps de la modification des facteurs de risque. Au moment de l'étude sur la sténose asymptomatique de l'artère carotide et des inclusions dans l'essai ACST-1, il n'y avait pas de protocole établi pour la réduction des facteurs de risque, et il n'y avait pas non plus d'utilisation généralisée des statines pour le traitement hypolipémiant et la réduction du risque cardiovasculaire. Cependant, le traitement par statines est associé à un risque réduit d'accident vasculaire cérébral et des évènements cardiovasculaires dans la prévention primaire et secondaire. KPNC a un programme établi pour gérer médicalement cette population à haut risque et dispose d'un mécanisme de suivi robuste pour l'observance des médicaments et d'autres paramètres pertinents. En conséquence, le détail des médicaments antihypertenseurs et hypolipémiants, à la fois au début et pendant le suivi, ont été colligés. Bien que l'observance ait été imparfaite, les indices pertinents (pression artérielle et taux de LDL) semblaient généralement bien contrôlés. Dans le modèle multivarié, toute utilisation de statines était significativement associée à un risque plus faible d'AVC. La mortalité totale était plus élevée, ce qui reflète probablement les efforts visant à inclure tous les patients atteints d'une maladie carotidienne et pas seulement les patients considérés comme des candidats chirurgicaux acceptables, comme on pourrait le voir dans une étude basée sur la chirurgie.
Limites
Cette étude a plusieurs limites. Premièrement, il n'y avait pas de méthode pratique pour évaluer les données d'imagerie brute comme cela pourrait être le cas dans un essai clinique, ni d'informations complètes sur l'accréditation des laboratoires vasculaires ou l'assurance qualité pendant la période d'étude. De plus, il n'y avait aucune information disponible concernant les caractéristiques de la plaque, que ce soit par échographie ou par imagerie par résonance magnétique, comme il est plus courant dans la pratique internationale.
Deuxièmement, l'utilisation de l'aspirine n'a pas été évaluée puisqu'il s'agit d'un médicament en vente libre et qu'il n'est pas spécifiquement suivi par les bases de données des pharmacies ou le dossier de santé électronique.
Troisièmement, bien que le codage du diagnostic d'AVC dans le dossier de santé électronique se soit avéré complet, l'évaluation des accidents ischémiques transitoires documentés n'était pas fiable et, par conséquent, l'effet d'un accident ischémique transitoire sur la composition et les résultats de la cohorte ne peut être pleinement pris en compte. Des difficultés de diagnostic et de documentation des accidents ischémiques transitoires ont déjà été signalées dans ce système de santé.
Quatrièmement, il existe un biais de sélection dans une étude de cohorte rétrospective comme celle-ci lorsque l'intervention est appliquée pour des raisons connues et inconnues. Les décisions de traitement et l'utilisation des ressources ne peuvent pas être prises en compte. Cette méthodologie a permis d'analyser en amont tous les patients présentant une imagerie carotidienne anormale et pas seulement ceux référés à une pratique spécialisée, capturant un groupe plus large de patients. En conséquence, les caractéristiques différentes entre le groupe chirurgie et le groupe traitement médical seul illustrent les différences de stratégie de traitement dans les préférences du patient et du soignant.
Cinquièmement, bien que la création de cette cohorte date maintenant de 12 à 13 ans, elle reste probablement pertinente pour l'ère actuelle étant donné que les soins de l'AVC dans le système de santé n'ont pas sensiblement changé depuis le début de l'étude.
CONCLUSION
Dans une cohorte communautaire de patients atteints de sténose carotidienne sévère asymptomatique qui n'ont pas subi d'intervention chirurgicale, le taux estimé d’infarctus cérébral lié à la carotide homolatérale était de 4,7 % sur 5 ans. Ces résultats peuvent éclairer la prise de décision concernant le traitement chirurgical et médical des patients atteints de sténose carotidienne sévère asymptomatique.
COMMENTAIRES
Cet article met en lumière 2 problèmes :
D’une part, il est difficile de maintenir des recommandations professionnelles sur la base d’études, certes randomisées et contrôlées, datant de plus de 20 ans, surtout quand, dans le même temps, la prise en charge a considérablement changé.
D’autre part, il n’est pas pertinent d’extrapoler à partir d’études randomisées contrôlées des taux d’évènements liés à une pathologie en raison des différents biais de sélection inhérents à toute étude randomisée, surtout quand un des bras comparateurs inclue la chirurgie. C’est ce biais qui nous a fait croire, à tort, que le degré de sténose carotidienne n’intervenait pas pour les lésions asymptomatiques (contrairement aux sténoses symptomatiques). Nous devons ce changement de paradigme à DPJ Howard et al (2).
La conclusion que nous devrions tirer est qu’il serait utile de faire une cohorte prospective sur la sténose de la carotide pour valider les résultats de RW Chang et al, et de reposer la question de la pertinence de la prise en charge interventionnelle de la sténose asymptomatique de la carotide. Sur la base de ce travail, un risque d’infarctus cérébral homolatéral à la sténose carotide de 0,9 % / an avec un bénéfice relatif de la chirurgie de 50 % nous amène à éviter 1 infarctus cérébral pour 200 carotides opérées, soit 99,5 % de chirurgie inutile : à méditer…
1.
Wong J, Taljaard M, Forster AJ, Escobar GJ, vanWalraven C. Derivation and validation of a model to predict daily risk of death in hospital. Med Care. 2011;49(8):734-743.
2.
Howard DPJ, Gaziano L, Rothwell PM; Oxford Vascular Study. Risk of stroke in relation to degree of asymptomatic carotid stenosis: a population-based cohort study, systematic review, and meta-analysis. Lancet Neurol. 2021 Mar;20(3):193-202. doi: 10.1016/S1474-4422(20)30484-1. Erratum in: Lancet Neurol. 2021 May;20(5):e4. PMID: 33609477; PMCID: PMC7889579.
