Rivaroxaban vs traitement anticoagulant standard dans la MTEV chez l’enfant : une étude randomisée contrôlée.
INTRODUCTION
L'incidence de la maladie thromboembolique veineuse (MTEV) chez l'enfant est estimée entre 0,01 et 0,05 pour 1000 enfants/an, ce qui est 20 à 100 fois moindre que chez l'adulte. Chez l'enfant, la physiopathologie de la thrombose, sa localisation anatomique et ses réponses pharmacologiques aux traitements anticoagulants diffèrent des adultes.
Depuis 1990, un seul essai randomisé dans une population pédiatrique (76 enfants) a été réalisé. Malheureusement, il a dû être interrompu en raison de la lenteur des inclusions. L’essai comparait l'héparine non fractionnée en intraveineux puis warfarine à l'héparine de bas poids moléculaire.
Jusqu’à présent, le traitement des thromboses veineuses de l'enfant était limité par l'absence de formulation anticoagulante adaptée à la population pédiatrique, la nécessité d'administrer le traitement par voie parentérale et la nécessité d'une surveillance biologique régulière.
Dans l’étude de phase 1 et 2 EINSTEIN-Jr, des schémas posologiques de rivaroxaban ajustés au poids corporel avec des comprimés ou une suspension orale nouvellement développée ont été établis pour les enfants, de la naissance à 18 ans ; ces « posologies pédiatriques » correspondent à la plage d'exposition biologique des jeunes adultes traités par 20 mg de rivaroxaban une fois par jour.
L’objectif de cette étude était de comparer l'efficacité et l'innocuité des schémas posologiques pédiatriques de rivaroxaban ajustés au poids corporel avec ceux des anticoagulants standards chez les enfants atteints de MTEV aigüe ayant reçu au moins 5 jours de traitement par héparine.
METHODE
Une étude de phase 3 randomisée en ouvert a été réalisée en comparant l'efficacité et l'innocuité du rivaroxaban avec celles des anticoagulants standards pour le traitement de la MTEV.
Les enfants pouvaient être inclus dans cette étude de la naissance à l'âge de 17 ans s'ils présentaient une MTEV confirmée et qu'un traitement par héparine avait été initié. Les enfants de moins de 0,5 ans devaient avoir un âge gestationnel à la naissance d'au moins 37 semaines, un poids corporel supérieur à 2600 g et avoir reçu une alimentation orale pendant au moins 10 jours.
Les enfants n'étaient pas éligibles s'ils présentaient un saignement actif ou présentaient un risque élevé de saignement contre-indiquant un traitement anticoagulant, avaient un nombre de plaquettes inférieur à 50 G/L, une maladie hépatique associée à une coagulopathie, une insuffisance rénale sévère ou une espérance de vie inférieure moins de 3 mois.
Le traitement était assigné de façon randomisée avec un rapport de 2:1 pour recevoir du rivaroxaban en ouvert ou des anticoagulants standards. La randomisation a été stratifiée selon les groupes d'âge et le site de MTEV (thrombose veineuse cérébrale, thrombose cave, ou rénale…), selon que la thrombose veineuse était liée à un cathéter, selon que la thrombose intéressait les membres inférieurs ou supérieurs, selon la présence d’une embolie pulmonaire ou la présence d’un thrombus dans le cœur droit.
Après 5 à 9 jours d'anticoagulation avec de l'héparine non fractionnée, de l'héparine de bas poids moléculaire ou du fondaparinux, les enfants ont été randomisés pour recevoir des anticoagulants standards ou du rivaroxaban. Les enfants alloués au rivaroxaban ont reçu une dose équivalente de 20 mg pour l’adulte ajustée au poids corporel, administrée une fois par jour (pour des poids corporels ≥ 30 kg), deux fois par jour (pour des poids corporels de 12 à < 30 kg) ou trois fois par jour (pour des poids corporels < 12 kg).
Le rivaroxaban a été administré sous forme de comprimés pelliculés à libération immédiate disponibles en dosages de 5, 10, 15 ou 20 mg ou en suspension. La suspension a été fournie sous forme de granulés dans un flacon qui a dû être rempli d'eau à une concentration de 1 mg/ml.
Les enfants du groupe des anticoagulants standards ont poursuivi le traitement par héparine ou sont passés à un antagoniste de la vitamine K, à la discrétion du clinicien.
À la fin de la période de traitement, une imagerie de la thrombose a été effectuée, à condition qu'aucun rayonnement ionisant supplémentaire ou anesthésie générale ne soit nécessaire.
La période de traitement de l'étude était de 3 mois, à l'exception des enfants de moins de 2 ans qui avaient une MTEV liée au cathéter, pour lesquels la période de traitement était de 1 mois.
Le critère principal d'efficacité était la récurrence d’un événement thromboembolique veineux symptomatique, évalué par un comité central indépendant d'adjudication. Le principal résultat d'innocuité était un critère composite de saignements majeurs et de saignements cliniquement pertinents non majeurs.
Les imageries répétées ont été comparées à celles du diagnostic et les résultats ont été classés comme normalisés (c.-à-d. Aucun thrombus résiduel observé), améliorés (c.-à-d. Thrombus toujours présent mais partiellement recanalisé ou impliquant moins de segments veineux), aucun changement pertinent (c.-à-d. Non recanalisé et d’extension similaire) ou détériorés (c.-à-d. Nouveau segment veineux impliqué).
RESULTAT
De novembre 2014 à septembre 2018, 500 enfants ont été inclus dans 28 pays. Neuf cas n’ont pas reçu le traitement de l'étude, un a été perdu de vue dans le groupe traitement standard. Les caractéristiques des patients sont présentées dans le tableau 1 ; 25% des enfants avaient des thromboses en lien avec un cathéter. Les thromboses veineuses étaient non provoquées dans 11% des cas. Les thromboses étaient provoquées par un facteur de risque persistant dans 17% des cas et un facteur de risque transitoire dans 47% des cas (tableau 2). Pour les thromboses veineuses survenues en présence d’un cathéter, 29% des patients avaient moins de deux ans et ont eu une période de traitement d'un mois. Les localisations des thromboses veineuses étaient les suivantes : thromboses aux membres inférieurs dans 33% des cas, thromboses au niveau des veines cérébrales dans 23% et au niveau des artères pulmonaires dans 16% des cas.
Dans le groupe traitement standard, 64% des patients ont eu un traitement par héparine seul et 34% héparine puis AVK. Le suivi médian était de 91 jours pour les enfants avec une période de traitement de trois mois et de 31 jours pour les enfants avec une période de traitement d'un mois.
Une récurrence symptomatique de MTEV est survenue dans 1% des cas dans le groupe rivaroxaban contre 3% dans le groupe anticoagulation standard. Il n'y a eu aucune MTEV fatale. Les résultats concernant la récurrence de la MTEV et des hémorragies sont présentés dans le tableau 3 ; 3% des patients du groupe rivaroxaban ont eu des épisodes de saignements cliniquement relevant, 2% dans le groupe contrôle ; le critère composite de récurrence de MTEV et de saignement majeur est survenu pour 1% des patients du groupe rivaroxaban et 4% des patients du groupe contrôle. Un enfant du groupe rivaroxaban est décédé du fait la progression de son cancer.
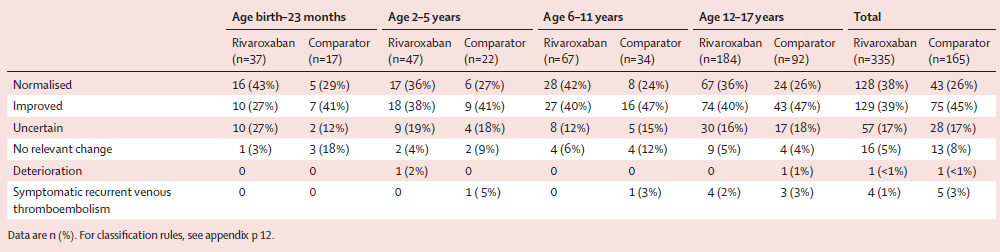
Les évolutions des thromboses veineuses en fonction de la tranche d'âge sont présentées dans le tableau 4.
Dans cette étude, le traitement de la MTEV chez l'enfant avec des posologies ajustées aux poids a montré que les risques de récidive thrombo-embolique et d’hémorragie significative étaient similaires au traitement anticoagulant standard. Il est possible que le traitement par rivaroxaban réduise davantage la masse thrombotique que le traitement standard.
En termes de tolérance, 70% des patients du groupe rivaroxaban et 62% des patients du traitement standard ont présenté des effets indésirables de grade I-II ; 12% et 14% respectivement de grade III et 1% dans chaque groupe des effets indésirables de grade IV sans qu'il y ait de différence significative entre les groupes. Les effets indésirables rapportés sont extrêmement hétérogènes et peuvent également se rencontrer au cours des pathologies sous-jacentes ayant favorisées la thrombose veineuse initiale.
DISCUSSION - CONCLUSION
Cette étude est la première depuis près de 30 ans à être parvenue à son terme dans cette problématique des thromboses veineuses de l’enfant à la phase aigüe. Il s’agit de la plus grande étude dans la MTEV de l’enfant. Elle montre que le traitement par rivaroxaban à une posologie ajustée au poids n'occasionne pas de sur-risque de récurrence de MTEV ou d'hémorragie significative par rapport aux traitements anticoagulants classiques.
Il faut être vigilant quant au schéma d'administration du rivaroxaban réalisé dans cette étude concernant la prise en charge à la phase aigüe de la MTEV de l’enfant. A la différence des posologies adultes, où un traitement est commencé d'emblée à 15 mg 2 x par jour pendant trois semaines puis 20 mg/jour, dans cette étude pédiatrique le traitement de la phase aigüe était une héparinothérapie pendant 5 jours suivi d'un traitement par rivaroxaban à une posologie équivalente à 20 mg/jour pour un adulte.
Le rivaroxaban pourrait être une option pour traiter les thromboses veineuses de l'enfant selon une posologie adaptée au poids. L’utilisation du rivaroxaban éviterait ainsi les contrôles biologiques répétés comme les injections sous-cutanées.
Tableau 1 : Caractéristiques des patients et localisations des thromboses veineuses.
Tableau 2 : Caractéristiques des profils de risque de MTEV.
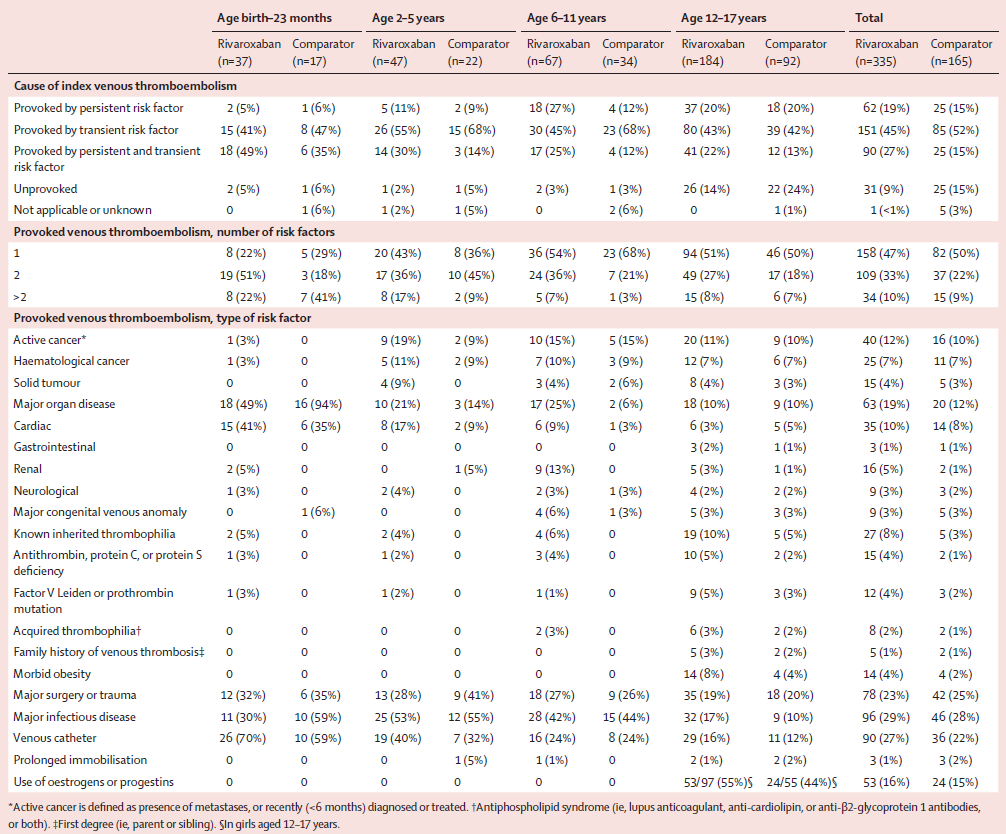
Tableau 3 : Récurrence de MTEV, manifestations hémorragiques au cours du suivi.
Tableau 4 : Évolution du thrombus en fonction des tranches d'âge chez les patients ayant eu des imageries répétées.